一、工艺流程
工艺流程见图1。各过程中主要反应举例如下:
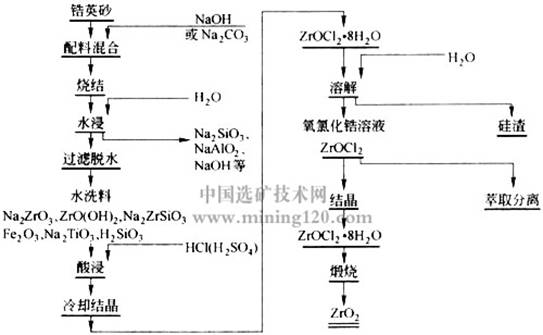
图1 碱分解锆英砂工艺流程
二、氢氧化钠烧结
主要反应:
ZrSiO4+2NaOH=Na2ZrSiO5+H2O
ZrSiO4+4NaOH=Na2ZrO3+Na2SiO3+2H2O
ZrSiO4+6NaOH=Na2ZrO3+Na4SiO4+3H2O
ZrSiO4+2Na2ZrSiO5=Na4Zr2Si3O12+ZrO2
ZrSiO4+Na2ZrO3=Na2Zr2SiO5+ZrO2
2ZrSiO4+3Na2SiO3=Na4Zr2Si3O12+Na2SiO5
反应过程中ZrSiO4与各反应物的反应速度为:
ZrSiO4/Na2ZrO3>ZrSiO4/Na4SiO4>
ZrSiO4/Na2SiO3>ZrSiO4/Na2ZrSiO5>
三、碳酸钠烧结
主要反应:
ZrSiO4+Na2CO3=Na2ZrSiO5+CO2
ZrSiO4+2Na2CO3=Na2ZrO3+Na2SiO3+2CO2
四、水浸
如果碱度不够,则部分发生下列水解反应:
Na2ZrO3+2H2O=ZrO(OH)2+2NaOH
Na2SiO3+2H2O=SiO2·H2O+2NaOH
五、盐酸浸出
Na2ZrO3+4HCl=ZrOCl2+2NaCl+2H2O
Na2ZrSiO3+4HCl=ZrOCl2+SiO2·2H2O+2NaCl
ZrO(OH)2+2HCl=ZrOCl2+2H2O
六、煅烧
ZrOCl2·8H2O=ZrO2+2HCl+7H2O
ZrO(OH)2·nH2O=ZrO2+(n+1)H2O
七、主要工艺条件
碱分解锆英砂制备锆、铪化合物的主要工艺条件见表1。
表1 碱分解锆英砂制备锆、铪化合物的工艺条件
|
工艺步骤 |
工 艺 条 件 |
备 注 |
|
烧结 |
ZrSiO4∶NaOH=1∶1.3(质量比);700~800℃,1.5h |
分解率95% |
|
ZrSiO4∶NaOH=1∶1.1(质量比);650℃,1~2h |
分解率90% | |
|
ZrSiO4∶NaOH=1∶(3~4)(摩尔比);600~700℃,2~3h |
分解率95% | |
|
ZrSiO4∶Na2CO3=1∶1.1(摩尔比);1050℃,2h |
||
|
水浸 |
1%~3% NaOH;60~80℃;20min;固液比(质量比)1∶5 |
水浸沉淀物Na2ZrO3,Na2ZrSiO5,ZrO(OH)2,Fe2O3,NaTiO3,H2SiO3;浸洗三次,除硅率大于98% |
|
酸浸 |
5~5.5mol/L HCl;100℃;ZrO2∶HCl=1∶5(摩尔比);0.5h |
锆转化率大于98% |
|
碱式硫酸锆水解析出① |
Zr4+=40~60g/L;70~80℃;HCl=1~1.5g/L;SO42-∶Zr4+=0.55∶0.6∶1(摩尔比) |
碱式硫酸锆组成为:2ZrO2·SO3·5H2O |
|
硫酸锆结晶析出② |
Zr4+=120~130g/L(对硫酸锆溶液); Zr4+=200~220g/L(对氧氯化锆溶液); VH2SO4浓∶VZr液=1∶2(体积比);洗液H2O∶H2SO4∶HCl=75∶40∶5(体积比) |
沉淀率94%~95%,沉淀物H2[ZrO(SO4)2]·3H2O |
|
煅烧 |
800~900℃ |
ZrO(OH)2·nH2O煅烧 |
|
800~900℃ |
ZrOCl2·8H2O煅烧 | |
|
850~900℃ |
2ZrO2·SO3·5H2O | |
|
850~900℃ |
H2[ZrO(SO4)2]·3H2O煅烧 |
① ② 用硫酸浸出的结果。
八、碱分解锆英砂的相关物化数据
图2~图5给出了HCl、H2SO4系中锆、铪的相关数据。
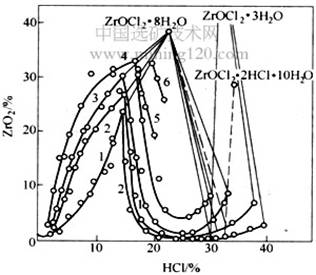
图2 ZrO2-HCl-H2O系中锆的溶解度
1-0℃;2-30℃;3-50℃;4-75℃;5~80℃;6~90℃
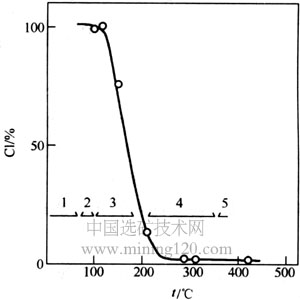
图3 ZrOCl2·8H2O热分解产物中氯含量与温度的关系
(287℃时[Cl]=2%;305℃时[Cl]≈0)
1-晶体结构不变;2-晶体结构发生小变化;3-晶体结构几乎不变;
4-非晶氧化锆;5-四方结构氧化锆
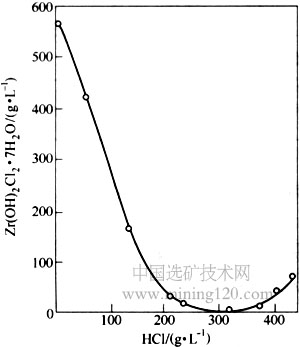
图4 Zr(OH)2Cl2·7H2O溶解度与HCl浓度的关系(20℃)
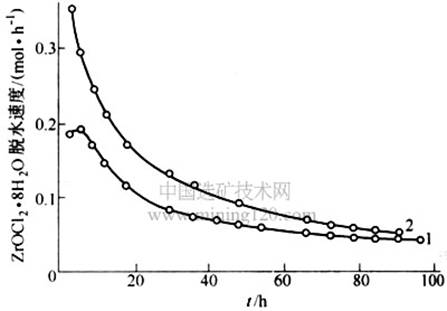
图5 ZrOCl2·8H2O脱水曲线
1-55℃;2-65℃
九、氧氯化锆的脱水机理
氧氯化锆ZrOCl2·8H2O脱水机理为:
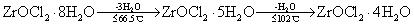
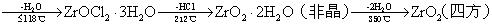
十、碱式硫酸锆的分解机理
碱式硫酸锆(2ZrO2·SO3·5H2O)的热分解机理为:
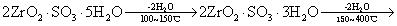
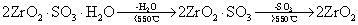
<600℃脱水,产品呈无定形;≈600℃产品组成约为ZrO2·0.57 SO3;>600℃开始分解出SO3,出现四方晶二氧化锆(T-ZrO2);1000~1050℃,SO3完全分解,产品呈单斜晶系;1150℃,单斜二氧化锆(M-ZrO2)重新转变为四方二氧化锆(T-ZrO2);由1150℃冷却至室温,样品又转化为M-ZrO2。
免责声明:矿库网文章内容来源于网络,为了传递信息,我们转载部分内容,尊重原作者的版权。所有转载文章仅用于学习和交流之目的,并非商业用途。如有侵权,请及时联系我们删除。感谢您的理解与支持。

